کم کاری مـادرزادی غــده تيـروئيــد و تشخیص علائم آن به سادگی
رشد و تکامل طبیعی غده تیروئید جنین و تولید هورمون تیروئید، برای تکامل مغز در دوران زندگی جنینی و پسازآن حیاتی است. غلظت هورمونهای تیروئید در گردش خون جنین در نیمه اول بارداری پائین است. در طی این دوران جنین بهطور کامل وابسته به هورمون تیروئید مادراست که از جفت عبور نموده و به جنین میرسد. تولید تیروگلوبولین در هفته 4 الی 6، احتباس ید در هفته 8 الی 10 و تولید هورمونهای تیروئید (تیروکسین و به نسبت کمتر تری یدو تیرونین) در غده تیروئید جنین در هفته 12 حاملگی شروع میشوند. بهطورکلی محور هیپو تالاموس- هیپوفیز – تیروئید جنین عملکرد خود را از نیمههای بارداری شروع نموده و در اواخر بارداری و بهنگام تولد به تکامل میرسد. کمبود هورمون تیروئید در طی دوران زندگی جنینی و یک سال اول بعد از تولد، با طیف وسیعی از اختلالهای عصبی– روانی (Neuropsychological disorders) توأم است. ارتباط بین عدم وجود غده تیروئید یا اختلال عملکرد آن با عقبماندگی ذهنی مقوله شناختهشده بسیار قدیمی است اما توصیف دقیق تظاهرات بالینی کمکاری شدید غده تیروئید که به آن کرتنیسم میگویند، اولین بار توسط Sir William Osler در سال 1897 میلادی صورت گرفت. حدود یک قرن پیش تأثیر عصاره تیروئید در برطرف نمودن علائم فیزیکی کمکاری مادر زادی غده تیروئید به اثبات رسید. بااینوجود عقبماندگی ذهنی این بیماران غیرقابلبازگشت بوده زیرابه علت تأخیر در تشخیص، درمان نیز با تأخیر و پس از گذشت زمان بحرانی رشد و تکامل مغز صورت میگرفت.
با شروع برنامه غربالگری کمکاری مادر زادی تیروئید نوزادان که منجر به شناخت زودرس مبتلایان در روزهای اول بعد از تولد و بلافاصله شروع درمان آنها میگردد، عقبماندگی ذهنی ناشی از این بیماری تحت کنترل درآمده است.
شیوع کمکاری مادر زادی تیروئید تا قبل از دوران غربالگری عمومی که تنها بر اساس یافتههای بالینی کشف میشدند یک مورد در 5 الی 10 هزار تولد متغیر بود... اولین برنامه غربالگری کمکاری مادر زادی تیروئید در سال 1974 میلادی در کبک کانادا آغاز شد. در اولین گزارش این برنامه که 175000 نوزاد را مورد غربالگری قرار داده بود میزان بروز بیماری بهطور تقریبی یک مورد در هر 6000 تولد تخمین زده شد. با گسترش برنامه غربالگری در کشورهای صنعتی، شرق اروپا، آمریکای جنوبی، آسیا و آفریقا میلیونها نوزاد سالانه مورد غربالگری برای کمکاری مادر زادی تیروئید قرار میگیرند. شیوع کمکاری مادر زادی تیروئید در کشورهای مختلف دنیا متفاوت بوده که ناشی از تأثیر میزان ید دریافتی مادران، تفاوتهای نژادی، عوامل ژنتیکی و روشهای غربالگری بکا ر گرفته میتواند باشد. بهطورکلی شیوع کمکاری مادرزادی تیروئید در یک منطقه با میزان ید رسانی در آن منطقه ارتباط نزدیک و مستقیم دارد. میزان بروز کمکاری مادر زادی تیروئید در آمریکا یک مورد در 3500 الی 5000 نوزاد، در اروپا یک مورد در 3000 تولد، در سوئد یک مورد در 6600 الی 7300 تولد و در ژاپن یک مورد در 5700 تولد گزارششده است. بهطورکلی شیوع این بیماری در آسیاییتبارها بیشتر بوده و در یونان یک مورد در 800 تولد نوزاد زنده گزارش گردیده است.
اولین مطالعه غربالگری کمکاری مادرزادی تیروئید در ایران توسط مرکز تحقیقات غدد درونریز دانشگاه علوم پزشکی شهید بهشتی در سال 1366 و قبل از اجرای برنامه غنیسازی نمک با ید در تهران و دماوند صورت گرفت ولی در سال 1368 به علت تعداد زیاد موارد فراخوان متوقف گردید. در این مطالعه اولیه میزان بروز بیماری یک مورد در هر 1000 نوزاد متولدشده به دست آمد که 3 تا 4 برابر میزان بروز آن در کشورهای پیشرفته جهان بود. با توجه به اینکه این مطالعه قبل از برنامه ید رسانی در کشور صورت گرفته بود احتمال میرفت که کمبود ید علت افزایش موارد فراخوان باشد. در سال 1372 همزمان با شروع برنامه ید رسانی همگانی مطالعه مشابه ای در شیراز و 5 شهر اطراف آن صورت گرفت که در این مطالعه نیز میزان بروز کمکاری مادر زادی تیروئید یک مورد در هر 1433 نوزاد متولدشده بود. با افزایش ید مصرفی خانوارهای ایرانی و اصلاح کمبود ید جامعه نیاز به شروع مجدد برنامه غربالگری کمکاری مادر زادی تیروئید احساس گردید و مرحله اول این طرح در سال 1376 در 5 بیمارستان دولتی تحت پوشش دانشگاه علوم پزشکی شهید بهشتی به مرحله اجرا درآمد که در طی 14 ماه حدود 3000 نوزاد مورد غربالگری قرار گرفتند که منجر به کشف 3 مورد کمکاری مادرزادی تیروئید گردید. درمجموع بر اساس مطالعات اولیه غربالگری در تهران شیراز و اصفهان میانگین بروز کمکاری مادر زادی تیروئید در کشور یک مورد در هر 1000 تولد نوزاد زنده تخمین زده شد.
شیوع بالای بیماری، عوارض جبرانناپذیر مغزی بیماری در صورت عدمتشخیص و درمان بهموقع که تنها با غربالگری دوران نوزادی قابلپیشگیری است و از طرف دیگر مقرونبهصرفه بودن اجرای برنامه در کشور مسئولین وزارت بهداشت درمان و آموزش پزشکی را بر آن داشت تا برنامه غربالگری را در سطح ملی به اجرا درآورند. لذا با استفاده از نتایج و تجارب بهدستآمده طرح غربالگری کمکاری مادر زادی تیروئید در سطح کشور بهعنوان یک برنامه ملی طراحی گردید و در سال 1382 در اولین برنامه کشوری بهطور آزمایشی در استانهای اصفهان، بوشهر و شهر شیراز اجرا شد و نهایتاً از سال 1384 این برنامه در سیستم سلامت کشور ادغامشده است. از زمان اجرای برنامه در سطح ملی تا آبان ماه سال جاری مجموعاً شش میلیون و هفتصد هزار نوزاد (49 درصد نوزاد دختر و 51 درصد نوزاد پسر) تحت غربالگری قرارگرفته که پانزده هزار نفر آزمودن غربالگری مثبت داشته و اقدامات تشخیصی و درمانی بر طبق دستورالعمل کمیته علمی کشوری برای آنان انجامشده است. این برنامه درمجموع حدود 95 درصد زایمانهای شهری و روستایی را تحت پوشش قرار داده و میزان فراخوان برنامه 9/2 در صد است.
تقسیمبندی کمکاری مادر زادی غده تیروئید
همانند کمکاری اکتسابی غده تیروئید، نوع مادرزادی آن را نیز میتوان بهصورت کمکاری اولیه (اختلال در خود غده تیروئید)، ثانویه (اختلال در غده هیپوفیز) و ثالثیِ (اختلال در غده هیپوفیز تالاموس) تقسیمبندی نمود. کمکاری مادرزادی غده تیروئید میتواند بهصورت گذرا و یا دائم باشد. نوع اولیه و دائم شایعترین نوع کمکاری مادر زادی غده تیروئید نوزادان بوده و در حقیقت شایعترین اختلال مادر زادی سیستم غدد درونریز بدن هست. حدود 80 تا 90 درصد علت کمکاری مادرزادی دائم غده تیروئید بهصورت تکگیر و ناشی از اختلال تکاملی غده تیروئید تحت عنوان دیسژنزی تیروئید است. این عنوان عدم وجود کامل یا تشکیل ناقص و تیروئید نابجا (Ectopic) را شامل میشود. 10 تا 20 درصد موارد ناشی از اشکال در تولید هورمونهای تیروئید (Dyshormogenesis) است. این اختلال میتواند در هر مرحله از تولید هورمون تیروئید از انتقال ید تا تشکیل تیروگلوبولین اتفاق افتد. این اختلالها بهصورت توارثی انتقالیافته و در ازدواجهای فامیلی شیوع بیشتری دارند. کمکاری دائمی غده تیروئید با منشأ مرکزی (اختلال در هیپوتالاموس یا هیپوفیز) بسیار نادر بوده و معمولاً یک در 50000 نوزاد را مبتلا میکند. این نوع از کمکاری مادر زادی غده تیروئید همیشه با کمبود سایر هورمونهای غده هیپوفیز یا هیپوتالاموس تالاموس توأم است.
انواع گذرای کمکاری مادرزادی غده تیروئید در مناطق دچار کمبود متوسط تا شدید ید شیوع دارند. در مناطق با دریافت ید کافی کمکاری گذرای غده تیروئید نوزادان میتواند ناشی از دریافت داروهای ضد تیروئید یا مواد حاجب رادیوگرافی توسط مادر در طی بارداری و یا استفاده از ضدعفونیکنندههای حاوی ید مثل بتادین بهنگام زایمان باشد. داروهای ضد تیروئید بهسرعت از خون پاکشده بنابراین سطح تیروتروپین (TSH) و تیروکسین آزاد این نوزادان در مرحله فراخوان (Recall) در محدوده طبیعی خواهند بود. انتقال آنتیبادیهای مهارکننده TSH مادر به جنین نیز یک علت نادر کمکاری گذرای غده تیروئید نوزاد است که تنها 1 تا 2 در صد موارد را شامل میشود. چون این آنتیبادیها به آهستگی از جریان خون نوزاد پاک میشوند لذا در مرحله فراخوان ممکن است نوزاد هنوز دچار کمکاری تیروئید باشد.
تظاهرات بالینی کمکاری مادر زادی غده تیروئید
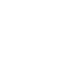
تنها معدودی از نوزادان مبتلابه کمکاری مادر زادی غده تیروئید بهنگام تولد یا در مرحله فراخوان علائم و نشانههای بالینی کمکاری تیروئید را بروز میدهند که شامل تأخیر در به دنیا آمدن، درشت پیکری، باز بودن فونتا نل خلفی، یرقان و تأخیر در تکامل سیستم اسکلتی هستند. درصد کمی از نوزادان دارای گواتر میباشند. سایر علائم و نشانهها شامل اشکال در تغذیه، هیپو ترمی، لتارژی، یبوست، یرقان طول کشیده دوران نوزادی، اتساع شکم، فتق نافی، پوست خشک، زبان بزرگ، گریه خشن و ظاهر پفآلود میباشند (شکل 1).
.png)
در صورت شک بالینی به کمکاری مادر زادی غده تیروئید نوزادان، بلافاصله اندازهگیری TSH و تیروکسین آزاد حتی اگر نوزاد بهنگام تولد تحت غربالگری قرارگرفته باشد، انجامشده و تا آماده شدن جواب نوزاد تحت درمان با قرص تیروئید قرار میگیرد.
نوزادان مبتلابه نوع مرکزی کمکاری مادر زادی غده تیروئید معمولاً دچار کاهش قند خون یا هیپو گلیسمی یا آلت تناسلی کوچک (میکرو پنیس) و بیضههای نهفته میباشند. وجود اختلال تکاملی مثل شکاف کام یا لبشکری و هیپو پلازی عصب اپتیک نیز ممکن است حاکی از اختلال در غده هیپوفیز باشند.
ارزیابیهای تشخیصی کمکاری مادر زادی غده تیروئید
غربالگری برای کمکاری مادر زادی تیروئید تنها راه رسیدن به تشخیص زودهنگام نوزادان مبتلا است. در برنامه غربالگری ملی ایران، نمونه خون از پاشنه پای نوزاد در روز 3 الی 5 بعد از تولد روی کاغذ فیلتر قرار داده میشود. کاغذ آغشته به نمونه خون نوزاد از طریق اداره پست به آزمایشگاه مرجع واقع در مرکز هر استان ارسال میگردد و در آنجا TSH نمونه خون موجود در کاغذ پالایه اندازهگیری میشود. چنانچه غلظت TSH بیشتر از 5 میلی یونیت در لیتر باشد نوزاد هر چه سریعتر فراخوان شده و یک نمونه خون وریدی برای اندازهگیری هورمونهای تیروئید جهت تائید تشخیص از وی گرفته میشود. نوزادان دچار کمکاری اثباتشده تیروئید تحت درمان مناسب قرارگرفته و برای ارزیابیهای تخصصی جهت تعیین علت بیماری نیاز به انجام اولتراسونوگرافی ناحیه گردن، اسکن تیروئید و رادیوگرافی از زانوها خواهند داشت.
درمان کمکاری مادرزادی تیروئید
تمام نوزادان دچار کمکاری مادر زادی غده تیروئید باید هر چه سریعتر با تجویز هورمون تیروئید مقادیر هورمونهای تیروئید خون آنها در محدوده طبیعی قرار گیرد. هدف درمان طبیعی نمودن غلظت تیروکسین سرم نوزاد در طی 2 هفته و TSH در طی یک ماه است. مقدار اولیه قرص لوتیروکسین 10 تا 15 میکروگرم به ازای هر کیلوگرم وزن نوزاد بوده که پس از خرد نمودن قرص پودر آن در آب یا شیر مادر حلشده و به نوزاد خورانده میشود. از مصرف همزمان ترکیبات آهن و مکملهای غذایی با قرص لوتیروکسین باید اجتناب نمود. در صورت استفاده از دوزهای بالاتر (12 تا 17 میکروگرم به ازای هر کیلوگرم وزن نوزاد) غلظت سرمی تیروکسین در طی 3 روز و TSH در طی 2 هفته به مقادیر هدف درمانی میرسند. با اندازهگیری تیروکسین آزاد سرم نوزاد یک هفته پس از شروع درمان میتوان افزایش مناسب غلظت سرمی آن را ارزیابی نمود. در طول 3 سال اول درمان غلظت سرمی تیروکسین کلی و آزاد باید در محدوده بالای مقادیر طبیعی و TSH در مقادیر پائین طبیعی حفظ شوند.
پی گیری کمکاری مادر زادی غده تیروئید
معاینات بالینی شامل ارزیابی رشد و نمو در طی 3 سال اول شروع درمان باید هرچند ماه یکبار انجام شوند. نوزادان دچار کم کاری مادر زادی غده تیروئید در معرض خطر ابتلا به ناهنجاریهای مادر زادی هستند (حدود 10 درصد در مقایسه با 3 درصد نوزادان سالم). ناهنجاریهای قلبی-عروقی شامل تنگی شریان ریوی، سوراخ بین دهلیزها یا بطنهای قلب شایعترین این ناهنجاریها میباشند.
در طول پی گیری غلظت تیروکسین سرم و TSH به شرح زیر اندازهگیری میشوند:
- در هفته 2 و 4 بعد از شروع درمان
- سپس به فواصل یک تا دو ماه در 6 ماه اول زندگی
- هر 3 تا 4 ماه بین 6 ماهگی تا 3 سالگی
- هر 6 تا 12 ماه تا کامل شدن رشد
- 4 هفته پس از هرگونه تغییر در دوز لوتیروکسین
علیرغم اهمیت درمان بهموقع و تداوم درمان کمکاری مادرزادی غده تیروئید که لزوم پی گیری مستمر این بیماران را ایجاب میکند، گزارشهایی حتی از کشورهای پیشرفته دنیا وجود دارد که مؤید کوتاهی در درمان و مراقبت نوزادان و کودکان مبتلابه کمکاری مادرزادی غده تیروئید است که نتیجه آن کاهش بهره هوشی و درجات مختلف عقبماندگی ذهنی بهویژه در دوران نوجوانی و جوانی است. بهمنظور پیشگیری از بروز هرگونه اختلال و کوتاهی در درمان صحیح این بیماران، آموزش والدین در جهت چگونگی مراقبت و پی گیری درمان فرزندانشان از ضروریات است.
مقالات مرتبط

شیوه های مدیریت چاقی و درمان آن بر اساس مقالات سال 2022
هدف از درمان چاقی این است که فرد کاهش وزن اولیهای در حدوده 10-5 درصد طی مدت 6 ماه داشته باشد و پس از این مرحله در 6 ماه بعدی وزن کاهش یافته تثبیت گردد. لازم به ذکر است یکی از خطاهای بسیار شایع در نظر گرفتن وزن ایدهآل به عنوان هدف اصلی میباشد.

اختلال چربی خون و بررسی جواب آزمایش ها و توصیف آن
چربی به طیف وسیعی از ترکیبات آلی گفته می شود که در کنار پروتئین و نشاسته (کربوهیدرات) یکی از سه نوع ماده مغذی در رژیم غذایی است. چربی یا بطور طبیعی در مواد غذایی از جمله گوشت، تخم مرغ، فرآورده های لبنی و روغن ها وجود داشته و یا بطور صناعی تحت عنوان چربی های ساختار یافته(Stru

کم کاری مـادرزادی غــده تيـروئيــد و تشخیص علائم آن به سادگی
تولید تیروگلوبولین در هفته 4 الی 6، احتباس ید در هفته 8 الی 10 و تولید هورمونهای تیروئید (تیروکسین و به نسبت کمتر تری یدو تیرونین) در غده تیروئید جنین در هفته 12 حاملگی شروع میشوند. بهطورکلی محور هیپو تالاموس- هیپوفیز – تیروئید جنین عملکرد خود را از نیمههای بارداری شروع
علائم بیماری هاشیموتو و روش های تخشیص و درمان
بیماری هاشیموتو یا تیروئیدیت مزمن لنفوسیتیک شایعترین نوع تیروئیدیت در انسان است. این بیماری نخستین بیماری خودایمنی است که در سال ۱۹۱۲ بهوسیله یک پزشک ژاپنی بنام هاکارو هاشیموتو کشف شد و بیماری به نام او ثبت گردیده است. در این بیماری مواد غیرطبیعی بنام آنتیبادی یا پادزهر ا

به مناسبت روز جهانی تيـــروئيـــد 2021
توصیه نهایی به آحاد جامعه نیز آن است که فقط از نمک ید دار تصفیه شده در حد متعارف استفاده نموده زیرا به مقدار کافی ید داشته و فاقد هر گونه ناخالصی است لذا کاملا بدون ضرر و عوارض جانبی است. هیچوقت از نمک دریا و سنگ نمک که تبلیغات نادرستی در مورد مصرف آنها می شود استفاده نکنند

آنتی بادی ضد گیرنده تیروتروپین(TSH) و بیماری گریوز نوزادی
مشخصه بیماریهای اتو ایمیون تیروئید وجود اتو آنتی بادی بر علیه اجزا مختلف غده تیروئید از جمله گیرندهTSH ، آنزیم پراکسیداز تیروئید(TPO) و تیروگلوبولین(Tg) است. در بین این اتو آنتی بادی ها، اتو آنتی بادی بر ضد گیرنده TSH بیشتر از همه با پاتوژنز بیماری همراه است.

نگاهی به تاریخچه کمبود ید در ایران
مشكل كمبود يد و اختلالهاي ناشي از آن در بسياري از مناطق ايران به عنوان يك بيماري آندميك شناخته شده بود .بررسي اپيدميولوژيك گواتر به عنوان يكي از شاخص ها ي عمده كمبود يد، نخستين بار در سال ۱۳۴۸ توسط انستيتو تغذیه در ايران صورت پذيرفت. یافته های به دست آمده نشان مي داد كه كمب

شیوه های مدیریت چاقی و درمان آن بر اساس مقالات سال 2022
هدف از درمان چاقی این است که فرد کاهش وزن اولیهای در حدوده 10-5 درصد طی مدت 6 ماه داشته باشد و پس از این مرحله در 6 ماه بعدی وزن کاهش یافته تثبیت گردد. لازم به ذکر است یکی از خطاهای بسیار شایع در نظر گرفتن وزن ایدهآل به عنوان هدف اصلی میباشد.

اختلال چربی خون و بررسی جواب آزمایش ها و توصیف آن
چربی به طیف وسیعی از ترکیبات آلی گفته می شود که در کنار پروتئین و نشاسته (کربوهیدرات) یکی از سه نوع ماده مغذی در رژیم غذایی است. چربی یا بطور طبیعی در مواد غذایی از جمله گوشت، تخم مرغ، فرآورده های لبنی و روغن ها وجود داشته و یا بطور صناعی تحت عنوان چربی های ساختار یافته(Stru

کم کاری مـادرزادی غــده تيـروئيــد و تشخیص علائم آن به سادگی
تولید تیروگلوبولین در هفته 4 الی 6، احتباس ید در هفته 8 الی 10 و تولید هورمونهای تیروئید (تیروکسین و به نسبت کمتر تری یدو تیرونین) در غده تیروئید جنین در هفته 12 حاملگی شروع میشوند. بهطورکلی محور هیپو تالاموس- هیپوفیز – تیروئید جنین عملکرد خود را از نیمههای بارداری شروع

علائم بیماری هاشیموتو و روش های تخشیص و درمان
بیماری هاشیموتو یا تیروئیدیت مزمن لنفوسیتیک شایعترین نوع تیروئیدیت در انسان است. این بیماری نخستین بیماری خودایمنی است که در سال ۱۹۱۲ بهوسیله یک پزشک ژاپنی بنام هاکارو هاشیموتو کشف شد و بیماری به نام او ثبت گردیده است. در این بیماری مواد غیرطبیعی بنام آنتیبادی یا پادزهر ا

به مناسبت روز جهانی تيـــروئيـــد 2021
توصیه نهایی به آحاد جامعه نیز آن است که فقط از نمک ید دار تصفیه شده در حد متعارف استفاده نموده زیرا به مقدار کافی ید داشته و فاقد هر گونه ناخالصی است لذا کاملا بدون ضرر و عوارض جانبی است. هیچوقت از نمک دریا و سنگ نمک که تبلیغات نادرستی در مورد مصرف آنها می شود استفاده نکنند

آنتی بادی ضد گیرنده تیروتروپین(TSH) و بیماری گریوز نوزادی
مشخصه بیماریهای اتو ایمیون تیروئید وجود اتو آنتی بادی بر علیه اجزا مختلف غده تیروئید از جمله گیرندهTSH ، آنزیم پراکسیداز تیروئید(TPO) و تیروگلوبولین(Tg) است. در بین این اتو آنتی بادی ها، اتو آنتی بادی بر ضد گیرنده TSH بیشتر از همه با پاتوژنز بیماری همراه است.

نگاهی به تاریخچه کمبود ید در ایران
مشكل كمبود يد و اختلالهاي ناشي از آن در بسياري از مناطق ايران به عنوان يك بيماري آندميك شناخته شده بود .بررسي اپيدميولوژيك گواتر به عنوان يكي از شاخص ها ي عمده كمبود يد، نخستين بار در سال ۱۳۴۸ توسط انستيتو تغذیه در ايران صورت پذيرفت. یافته های به دست آمده نشان مي داد كه كمب